گاز هلیوم
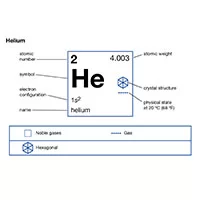
هلیوم (He) ، عنصر شیمیایی ، گاز بی اثر گروه 18 (گازهای نجیب) جدول تناوبی. دومین عنصر سبک (فقط هیدروژن سبک تر است) ، هلیوم یک گاز بی رنگ ، بی بو و بی مزه است که در دمای 268.9 درجه سانتیگراد (452 درجه فارنهایت) مایع می شود. نقاط جوش و انجماد هلیوم پایین تر از سایر مواد شناخته شده دیگر است. هلیوم تنها عنصری است که با خنک کننده کافی در فشار معمولی اتمسفر نمی تواند جامد شود. لازم است فشار 25 اتمسفر در دمای 1 K (272 درجه سانتیگراد یا 458 درجه فارنهایت) اعمال شود تا آن به فرم جامد آن تبدیل شود.
| atomic number | 2 |
| atomic weight | 4.0026 |
| melting point | none |
| boiling point | −268.9 °C (−452 °F) |
| density (1 atm, 0 °C) | 0.1785 gram/litre |
| oxidation state | 0 |
| electron configuration | 1s2 |
تاریخچه:
هلیوم توسط ستاره شناس فرانسوی پیر جانسن ، که در طوفان سال 1868 ، یک خط زرد روشن را در طیف کروموسفر خورشیدی کشف کرد ، در فضای گازی اطراف خورشید کشف شد. این خط در ابتدا فرض شد که عنصر سدیم را نشان می دهد. در همان سال ، ستاره شناس انگلیسی ، جوزف نورمن لاکایر ، یک خط زرد را در طیف خورشیدی مشاهده کرد که مطابق با خطوط شناخته شده D1 و D2 سدیم نیست ، و به همین دلیل او آنرا خط D3 نامید. لاکایر نتیجه گرفت که خط D3 ناشی از عنصری در خورشید است که بر روی زمین ناشناخته است. او و شیمیدان ادوارد فرانکلند در نامگذاری این عنصر از واژه یونانی Sun، hēlios استفاده کردند. شیمیدان بریتانیایی سر ویلیام رامسی در سال 1895 وجود هلیوم روی زمین را کشف کرد. رامسی نمونه ای از Cleveite معدنی حاوی اورانیوم را بدست آورد و با بررسی گاز تولید شده با گرم کردن نمونه ، متوجه شد که یک خط زرد روشن بی نظیر در آن وجود دارد. طیف با خط D3 مشاهده شده در طیف خورشید مطابقت دارد. بنابراین عنصر جدید هلیوم به طور قطع مشخص شد. در سال 1903 ، رامسى و فردریک سوددی بیشتر مشخص كردند كه هلیوم محصول جداشدن خود به خود از مواد رادیواكتیو است.
فراوانی ها و ایزوتوپ ها
هلیوم حدود 23 درصد از جرم جهان را تشکیل می دهد و به همین دلیل از نظر هیدروژن موجود در کیهان در رتبه دوم قرار دارد. هلیوم در ستارگان متمرکز شده است ، جایی که با ترکیب ذرات هسته ای از هیدروژن سنتز می شود. اگرچه هلیوم در جو زمین فقط به میزان 1 قسمت در 200000 (0.0005 درصد) رخ می دهد و مقادیر کمی در مواد معدنی رادیواکتیو ، آهن شهاب سنگ و چشمه های معدنی رخ می دهد ، حجم زیادی از هلیوم به عنوان یک جزء (تا 7.6 درصد) در گازهای طبیعی در ایالات متحده (به ویژه در تگزاس ، نیومکزیکو ، کانزاس ، اوکلاهما ، آریزونا و یوتا). وسایل کمتری در الجزایر ، استرالیا ، لهستان ، قطر و روسیه کشف شده است. هوای معمولی تقریباً 5 قسمت در هر میلیون هلیوم دارد ، و پوسته زمین تنها در حدود 8 قسمت در هر میلیارد است.
هسته هر اتم هلیوم حاوی دو پروتون است ، اما همانطور که در مورد همه عناصر وجود دارد ، ایزوتوپ های هلیوم نیز وجود دارند. ایزوتوپهای شناخته شده هلیوم حاوی یک تا شش نوترون هستند ، بنابراین تعداد جرم آنها بین سه تا هشت است. از بین این شش ایزوتوپ ، فقط آنهایی که دارای تعداد انبوهی از سه (هلیوم -3 ، یا 3He) و چهار (هلیوم -4 یا 4He) هستند ، پایدار هستند. همه بقیه رادیواکتیو هستند و به سرعت در مواد دیگر پوسیده می شوند. هلیومی که در روی زمین وجود دارد یک جزء اولیه نیست بلکه با پوسیدگی رادیواکتیو ایجاد شده است. ذرات آلفا ، که از هسته مواد رادیواکتیو سنگین تر خارج می شوند ، هسته ایزوتوپ هلیوم 4 هستند. هلیوم به مقدار زیادی در جو تجمع نمی یابد زیرا جاذبه زمین برای جلوگیری از فرار تدریجی آن به فضا کافی نیست. ردیابی ایزوتوپ هلیوم 3 روی زمین ناشی از فروپاشی منفی بتا ایزوتوپ نادر هیدروژن 3 (تریتیوم) است. هلیوم -4 بسیار نزدیک ترین ایزوتوپهای پایدار است: اتمهای هلیوم -4 از تعداد هلیوم 3 در حدود 700000: 1 در هلیوم جوی و در حدود 7000،000: 1 در بعضی از مواد معدنی حاوی هلیوم می باشد.
خصوصیات
هلیوم -4 با داشتن دو شکل مایع بی نظیر است. فرم مایع معمولی هلیوم I نام دارد و دمای آن از دمای جوش 4.21 درجه سانتیگراد (268.9 درجه سانتیگراد) تا حدود 2.18 درجه سانتیگراد (271 درجه سانتیگراد) وجود دارد. در زیر 2.18 K ، هدایت حرارتی هلیوم -4 بیش از 1000 برابر بیشتر از مس می شود. به این شکل مایع هلیوم II گفته می شود تا آن را از هلیوم مایع معمولی متمایز کند. هلیوم دوم خاصیتی به نام ابرفلوئید را نشان می دهد: ویسکوزیته آن ، یا مقاومت در برابر جریان ، آنقدر کم است که اندازه گیری نشده است. این مایع در یک فیلم نازک روی سطح هر ماده ای که لمس می کند پخش می شود و این فیلم حتی بدون اصطکاک حتی در برابر نیروی گرانش جریان می یابد. در مقابل ، هلیوم 3 بسیار کمتر ، سه مرحله مایع قابل تشخیص را تشکیل می دهد که دو مورد از آنها سطحی هستند. نقره فوق العاده در هلیوم 4 توسط فیزیکدان روسی پیوتر لئونیدوویچ کاپیتسا در اواسط دهه 1930 کشف شد و همین پدیده در هلیوم 3 برای اولین بار توسط داگلاس D. اوشرف ، دیوید م لی و و رابرت سی ایالت ریچاردسون در سال 1972 مشاهده شد.
نمودار فاز هلیوم 3 نشان می دهد که حالت های ایزوتوپ پایدار هستند. Enyclyclopædia Britannica، Inc.
مخلوط مایع از دو ایزوتوپ هلیوم 3 و هلیوم 4 که در دمای کمتر از 0.8 K (272.4 درجه سانتی گراد ، یا 458.2 درجه فارنهایت) به دو لایه جدا می شود. یک لایه عملا هلیوم -3 خالص است. مورد دیگر بیشتر هلیوم -4 است اما حدود 6 درصد هلیوم -3 را حتی در کمترین دما به دست می آورد. انحلال هلیوم 3 در هلیوم 4 با یک اثر خنک کننده همراه است که در ساخت کریستات ها (دستگاه هایی برای تولید درجه حرارت بسیار پایین) ورد استفاده قرار گرفته است که می تواند دمای هوا را به دست آورد و آن را برای روزها حفظ کند و کمترین مقدار آن برابر با 0.01 K باشد 273.14) درجه سانتیگراد یا 459.65 درجه فارنهایت(.
تولید و استفاده
گاز هلیوم (98.2 درصد خالص) با مایع سازی سایر اجزاء در دماهای پایین و تحت فشارهای زیاد از گاز طبیعی جدا شده است. جذب سایر گازهای موجود در ذغال سنگ خنک شده و فعال شده 99.995 درصد هلیوم خالص را به همراه دارد. مقداری هلیوم از مایعات هوا در مقیاس وسیع تأمین می شود. مقدار هلیوم حاصل از 1000 تن (900 تن) از هوا حدود 112 فوت مکعب (3.17 متر مکعب) است ، همانطور که در دمای اتاق و فشار اتمسفر اندازه گیری می شود.
هلیوم به عنوان یک گاز بی اثر برای جوش فلزات مانند آلومینیوم استفاده می شود. در پیشرانه موشک (برای تحت فشار قرار دادن مخازن سوخت ، به ویژه آنهایی که برای هیدروژن مایع وجود دارند ، زیرا تنها هلیوم در دمای هیدروژن مایع هنوز گاز است). در هواشناسی (به عنوان گاز بالابر برای بالن های حامل ابزار). در دماهای پایین (به عنوان یک مایع خنک کننده زیرا هلیوم مایع سردترین ماده است)؛ و در عمل تنفس فشار قوی (مخلوط با اکسیژن ، مانند کارهای غواصی و کار Caisson ، به ویژه به دلیل حلالیت کم در جریان خون( از هلیوم برای اندازه گیری قدمت شهاب سنگ ها و سنگ ها استفاده می شود.